「遺伝子組換え技術」とは、ある生物がもつ遺伝子情報の一部を、他の生物の細胞に導入して、その遺伝子を発現させる技術のことです。品種改良された遺伝子組換え作物等はこの技術を応用しています。最近では、「ゲノム編集」というワードも話題になっていますね。今回は遺伝子組み換え技術やゲノム編集について触れてみようと思います。
遺伝子工学の歴史
DNA(デオキシリボ核酸)が生物の種の存続や成長、維持に欠かせないものだという事は周知の事実だと思われます。そこで、この章では遺伝情報物質としてDNAが証明された頃から今日に至るまでの遺伝子工学の発展について簡単に振り返りながら説明したいと思います。
1944年 DNAが遺伝子の実体であることの証明
情報の伝達する分子として核酸が発見は、酵素が生物反応の触媒である事を証明したEduard Buchner (1860-1917)や、酵素反応の「鍵と鍵穴説」を提唱したEmi Fischer (1852-1919)らの実験から半世紀遅れの出現でした。1944年、Oswald Avery, Colin MacLeod, Maclyn McCartyは肺炎連鎖球菌の有毒株からDNAを抽出し、抽出したDNAを同じ最近の無毒株と混合した。この操作の結果、無毒株は持続的な有毒株に形質転換し、DNAが遺伝物質であるという決定的な証拠を示す実験となった。
さらに詳しく
1952年、HersheyとChaseによってバクテリオファージを用いた実験が行われ、DNAが遺伝物質であるということが示されました。高校生物にも頻繁に出題する有名な実験ですね。
1953年 DNAの三次元構造の提唱
1953年、James D WatsonとFrancis H. C. Crickらによって、DNAが「4種の単位分子ATGCの連続によってできたDNA分子が2本寄り合わさって出来た二重らせん構造である」と提唱された。また、DNAが自己複製し、それによって次世代に生体情報を伝達できることも分かった。その後の研究により、DNAに暗号化されている情報はリボ核酸(RNA)に転写され、次にタンパク質に翻訳されることが示された。
ココがポイント
DNA→(転写)RNA→(翻訳)タンパク質
1972年 組み換えDNAの作製
1972年Stanley N. CohenとHerbert Boyerによって細菌DNAとプラスミドを使って初めての組み換えDNAが作製された。これまで自然に生じた組み換えDNA分子が遺伝子研究に利用されてきたが、1970年代に特定の遺伝子を同定し、単離するための汎用的な研究方法が開発されていく。
1996年 ゲノム編集ツールであるDNA切断酵素の開発
遺伝子の変異を回避するために、DNAの塩基配列を特異的に切断する方法の開発が重要であると考えられた。そこで開発されたのが、特定の塩基配列を認識・切断する人工の制限酵素「ZFN」である。のちに様々な人工の制限酵素が開発される。
2003年 ヒトゲノム化計画
ヒトゲノム計画とは国際的な研究協力であり、ヒトの全ゲノムの塩基配列の決定と解析を行うことを究極の目的とした。この計画には多くの国と研究者が関与しており、2003年4月、国際ヒトゲノム配列解析共同体はヒトゲノムのほぼ完全な配列を決定した。ヒトゲノムの塩基配列を知ることは、5000を超える遺伝病の多く、または遺伝的素因が何らかの働きをしている病態の多くについて、その緩和や治療に貢献することに繋がると期待されている。
組み換えDNA技術の応用
核酸のバイオテクノロジーの応用は、基礎研究から遺伝子治療まで多岐にわたる。特に農業の分野で遺伝子工学は活発で、遺伝子の改変により生産性の向上や品質改善、昆虫や病気に抵抗性を持つものなどの植物が生み出されている。日本では、ダイズ、トウモロコシ、ナタネ、ジャガイモ、綿などの輸入販売が許可されている。

T-DNAクローニングの技術により、植物の葉緑体や核のゲノムに除草剤に耐性をもつ遺伝子を導入することが出来た。同様に、昆虫に対する毒素の遺伝子を植物に導入して昆虫の被害に対して耐性をもたせることも行われている。図は昆虫に耐性のトマトの苗木。左側の苗木はトマトにつく昆虫に毒性をもつ細菌のタンパク質をコードする遺伝子を持っている。右は野生型で、その昆虫がつくと成長ができない
また、哺乳類などの大きな多細胞生物に外来DNAを組み込んで作製するトランスジェニック生物を用いてヒトの特定の疾患を標的にした研究も可能となり、正常と病気の細胞や組織の差を明確にし、何が病気を引き起こすのかを理解することができるようになると期待されている。
中でも、2006年に京都大学の山中伸弥先生によって誕生したiPS(induced pluripotent stem cell) 細胞は、ごく少数の遺伝子を導入し培養することで様々な組織や臓器の細胞に分化する「人工多能性幹細胞」です。ES細胞のように特定の細胞からではなく、皮膚や血液などの比較的採取しやすい体細胞から作製することが可能なため、自身の細胞から作製すれば拒絶反応が起こりにくいと言われています。今後、iPS細胞を用いた研究は、ヒトの病気のメカニズムを解明し、病気の進行を止めたり、あるいは治癒する薬剤の探究への応用が期待されています。iPS細胞について詳しく知りたい方は、京都大学のiPS細胞研究所のHPをご参照ください。リンクはこちら
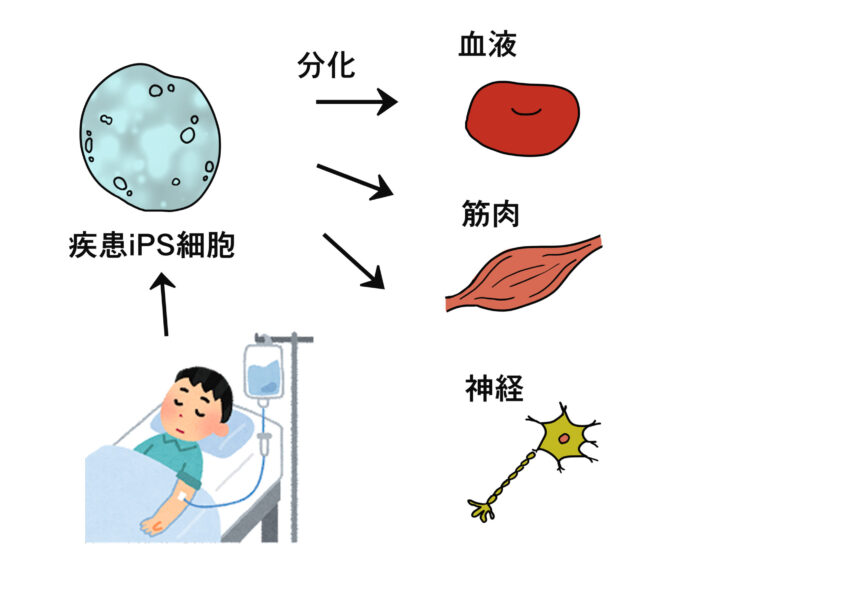
遺伝子治療用医薬品、iPS細胞を用いた組織再生のための開発も進んでいる。遺伝子改変植物で作られる医薬品もある。図のように疾患iPS細胞を用いた創薬研究も進められており、希少疾患や神経難病などの原因遺伝子の解明、新薬開発に大きな期待をされている。
遺伝子組み換えとゲノム編集の違い
「成長スピードが速くなるよう改良した高級魚のトラフグ」、「身の量が多い鯛」、「血圧を下げる成分の多いトマト」といった「ゲノム編集食品」が注目を浴びています。DNAに人の手を加えることで、思い通りの特徴を出すことも可能な時代となってきましたが、遺伝子組み換えとの違いは?
ゲノム編集とは?
「ゲノム編集」は、生物のDNA、遺伝子、ゲノムをいじる操作であり、遺伝子工学の一種。文字通り、DNAを編集しますが、今のところ「編集作業」が許可されているのは①不要なゲノムの削除 ②ゲノムの配列順序の変更のみである。つまり、ゲノム編集の前後を通じて、DNAに余計なゲノム(=他の生物の遺伝情報)は加えられていない。「身の多い鯛」に関しても、もともとの鯛に組み込まれていた「筋肉量をある程度以上に増やさない」というゲノムを削除したためである。
遺伝子組み換えとゲノム編集の違い
ゲノム編集
狙った遺伝子(特定のDNA配列)を直接切るなどして変異させるため、思い通りの特徴を発現させやすい。DNAの特定の場所を狙って切るハサミの役目をするのが、「人工ヌクレアーゼ」というDNA切断酵素です。
遺伝子組み換え
他の生物の遺伝情報を導入する。生物AのDNAから優れた遺伝子aを化学的に切り取り、生物Bの細胞内に導入するとBにAの性質が現れる。思い通りに組み込まれない場合があり、作るのに時間がかかる。意図しない変化が起きる可能性もあり。
遺伝子組み換え生物に関する日本の規制
日本に遺伝子組み換え生物を輸入、流通、栽培その他使用をする際は、事前に使用の目的に従って以下の法律に基づき、科学的に安全性を審査し、問題が乗じないと評価されて初めて使用できる仕組みとなっている。※農林水産省のHP参照
- 食品としての安全性は「食品衛生法」
- 飼料としての安全性は「飼料安全法」
- 生物多様性への影響は「カルタヘナ法」
今回は、3つ目の「カルタヘナ法」に関して詳しく紹介しようと思います。
カルタヘナ法とは
カルタヘナ法とは、生物多様性を確保するために制定された法律(日本では2004年に施行)で、遺伝子組換え生物が生物多様性に影響を及ぼさないかどうかの審査や使用方法が定められている。この法律により、安全性が確認されるまでは、遺伝子組換え生物の屋外での栽培や生育は禁止される。遺伝子組換え生物の使用等については、以下に掲げる行為が対象となる。
- 食用、飼料用、実験材料等に供するための使用
- 栽培、飼育、培養等の育成
- 加工
- 保管、運搬、廃棄
また、上記に付随する行為も全て対象となる。
カルタヘナ法では、遺伝子組換え生物の使用形態を以下のように2種類に分け、それぞれのアプローチで生物多様性への影響を防止している。
- 第一種使用(開放系での使用):食料や飼料としての運搬、農地での栽培など。生物多様性への影響が生ずる恐れがないと承認されたものが使用可能。
- 第二種使用(閉鎖系での使用):拡散防止機能を有する実験室や工場など。拡散防止措置が適切かどうかの確認を受ける必要がある
ココに注意
研究等に使用される遺伝子組み換え培養細胞は、規制の対象外となる。ただし、遺伝子導入した培養細胞およびトランスジェニックマウスやノックアウトマウスから分離・調整した細胞を別のマウス等に移植する実験は、遺伝子組換え実験に該当する。
最後に
ここまで見て頂きありがとうございました。遺伝子組換えやゲノム編集は賛否両論の意見がありますが、難病に苦しむ人達の新薬や治療、また再生医療への発展に大きく貢献してくれているのも事実です。安全性を確保しつつ、きちんとした環境下での取り扱いが重要です。
以下参考サイト/参考書籍となります
参考
ホートン生化学 第4版 / 身近にあふれる「化学」が3時間でわかる本 / 農林水産省HP
